醫學院袁健團隊合作研究揭示高階DNA修復拓撲結構的調控機製,相關研究成果發表於《分子細胞》
來源:醫學院
時間:2023-03-01 瀏覽🎇:
2月27日↙️,恒达平台醫學院袁健教授團隊聯合美國梅奧醫學中心樓振昆團隊,在《分子細胞》(Molecular Cell)雜誌在線發表了題為“SLFN5-mediated chromatin dynamics sculpt higher-order DNA repair topology”的文章。黃金舟博士和恒达的吳晨明博士作為共同第一作者🧁📦。

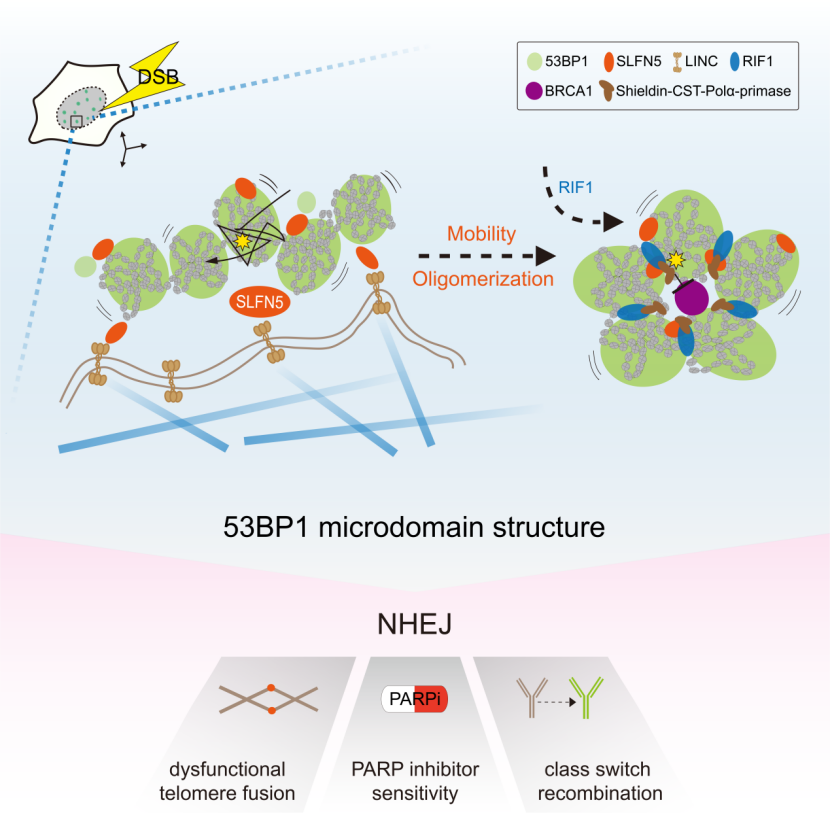
該研究探索了53BP1在DNA斷端高階拓撲排列的關鍵因素,並提出53BP1-MD高階結構的塑造需要SLFN5介導的兩個過程:(1) 由SLFN5-LINC-微管軸驅動的染色質運動, (2) 由SLFN5調控的53BP1寡聚體的組裝👙。總之,這項研究確立了SLFN5是聯系DNA斷端染色質動態變化和拓撲重排的關鍵調節器,並提出染色質動態變化塑造高階DNA修復拓撲結構的調控模型。
研究首先發現SLFN5在53BP1的鄰近標記蛋白質組網絡中與SHLD3處於相同的高置信度亞組,提示SLFN5可能是53BP1通路的潛在作用分子👆。生化實驗和鄰近連接技術進一步驗證了SLFN5與53BP1相互作用👯♀️,並且SLFN5的相互作用網絡擴展到其他NHEJ分子,包括RIF1,PTIP和Shieldin復合體亞基。通過分析乳腺癌病人的基因組WGII (Weighted genome integrity index) 信號,發現SLFN5低表達的病人基因組WGII信號上升🧑💻,提示SLFN5低表達會對基因組穩定性產生消極影響👩🎓。
接下來,研究發現SLFN5到DSB損傷位點的招募依賴於53BP1🍐,但不依賴於下遊分子RIF1和REV7🤏。另一方面,SLFN5不影響53BP1,RIF1和Shieldin復合體到DSB損傷位點的招募,表明SLFN5可能處於與RIF1-Shieldin不同的功能模塊中。值得註意的是🔥,SLFN5缺失導致BRCA1到DSB損傷位點的招募和Foci形成的強度顯著增加👨🌾。作者由此應用超分辨率顯微鏡對BRCA1和53BP1蛋白進行可視化研究。作者發現在傳統顯微鏡下顯示的SLNF5缺失導致BRCA1 foci增強🧑🏻🦲,在超高分辨率顯微鏡下顯示出BRCA1在空間上的擴散分布🛋。有意思的是🐽,與野生型在響應DSB修復形成的環狀高階結構相比較🤌🏼🤦♂️,SLFN5缺失極大擾亂了53BP1-MD的形成🧼,顯示為無序的53BP1-NDs排布和拓撲結構的改變。進一步研究顯示,當DSB損傷發生時,SLFN5被招募到53BP1-MD高階結構的界面和邊界處。SLFN5的招募動力學與53BP1類似,出現在DNA斷裂的早期,並且在隨後的1小時內達到峰值。這些數據說明,SLFN5調節了53BP1-MD組裝的最初過程。此外,作者在功能障礙的端粒中也觀察到53BP1-MD高階結構,且SLFN5缺失導致此端粒上的拓撲結構被破壞。這些數據表明🥎,SLFN5是53BP1-MD高階結構的關鍵調控分子🧑🦯➡️。
研究進一步探索SLFN5與53BP1相關功能之間的聯系🙆🏻♂️。他們發現,Slfn5 基因敲除(Knockout,KO)可以極大抑製由NHEJ介導的功能障礙端粒 (端粒保護蛋白Trf2-KO)的融合。來自Slfn5-KO小鼠胚胎的MEFs顯示比野生型更多的染色體異常斷裂。通過對Slfn5-KO小鼠的脾臟進行分析發現γH2AX信號的顯著積累,同時血液中紅細胞的微核數目也出現顯著增加。這些數據進一步表明SLFN5與基因組穩定性的維持密切相關。接下來,作者發現Slfn5-KO小鼠中B細胞的抗體類型轉換重組(Class switch recombination, CSR)的過程被抑製💭。同時,在BRCA1-KO的細胞中😸,SLFN5的缺失可以恢復HR及DNA斷端的切除效率,並使細胞對PARP (poly (ADP-ribose) polymerase) 抑製劑重新耐受🌒🗝。此外🏄🏽♀️,作者發現SLFN5缺失導致HR的增加並抑製NHEJ的修復☛,提示SLFN5參與DSB修復途徑的選擇。這些結果表明💑,SLFN5是NHEJ途徑的關鍵分子🧑🍼,並且SLFN5與53BP1在功能上具有遺傳上位性 (Genetic epistasis)。
SLFN5 的N端推測具有核酸酶活性,C端具備Walker A和Walker B結構域,提示具有解旋酶活性和ATP酶活性🧑🏼🎤。作者通過構建不同的酶活突變體發現🏌🏽♀️,SLFN5的ATP酶活性對於53BP1-MD的組裝和SLFN5在NHEJ的功能是不可或缺的📉。53BP1通過招募SLFN5到DNA斷端來促進其高階結構形成,那麽53BP1是否存在一個具體的區域負責SLFN5的招募👇🏽?作者通過引入不同的53BP1截斷體🚣🏼♂️,將參與SLFN5招募的區域範圍縮小到了Mob (影響53BP1介導的染色質運動) 和Core (影響53BP1寡聚化的形成) 的區域。這些數據提示SLFN5可能參與的是53BP1依賴的染色質運動和寡聚化🧜🏻♂️。接下來,通過對受損傷染色質移動性的分析,作者發現👨🏻⚕️,DNA斷端染色質的運動受到SLFN5的嚴格調控,這一過程需要53BP1 Mob區域的相互作用和SLFN5 的ATP酶活。與此同時🙅🏿♂️,SLFN5的缺失也會極大影響53BP1寡聚化的形成🔰。有意思的是💘👩🏽✈️,將53BP1的Mob或Core區域進行突變都可以破壞53BP1-MD高階結構。同時,作者發現,Mob和Core區域的雙突變可以破壞53BP1對DNA斷端的保護作用。這些數據說明,53BP1介導的染色質動態變化是其形成高階拓撲結構的必要條件。
先前研究發現微管-LINC復合體促進53BP1調節的染色質運動,盡管LINC如何與53BP1進行連接並不清楚,可能中間存在一個X因子🧑🏼🍼。基於上述實驗結果,作者探索SLFN5作為連接的X因子的可能性。通過對微管的化學擾動,可以發現53BP1-MD高階結構的紊亂👱🏽。此外🤘🏼,LINC復合體亞基SUN1和SUN2與SLFN5強烈相互作用,並且SUN1和SUN2的缺失擾亂53BP1-MD高階結構,這與SLNF5缺失導致的表型類似👧🏼🌔。這些結果表明🐕,微管-LINC復合物促進DNA斷端的移動性,並驅動了53BP-MD的拓撲排列👨🏿⚖️,而這一過程由SLFN5介導🎁。
總的來說,該研究發現SLFN5是調節53BP1在DNA斷端形成高階拓撲結構的關鍵分子。當DSBs觸發53BP1圍繞染色質形成納米域 (ND) 時🫶🏽🚵🏿♂️,SLFN5促進受損染色質運動和53BP1的寡聚化👐🏻,促使形成更高階的53BP1微米域 (MD)。RIF1隨後穩定了這一拓撲結構。SLFN5的缺失會導致53BP1-MD的拓撲結構被破壞,引起BRCA1在染色質的過度彌散,導致DNA斷端的過度切除和影響基因組的穩定性。該研究表明SLFN5和RIF1在53BP1這一空間事件上存在時間差異性🍰👁🗨。與RIF1的晚期招募行為相比較👅,SLFN5的招募與53BP1幾乎同時發生,並主要定位在53BP1-MD的界面和邊界處🔝,因此認為SLFN5的招募主要調節53BP1-MD拓撲重排的最初步驟,而53BP1-MD一旦形成🍐,RIF1有助於維持該結構的穩定。
論文鏈接:https://doi.org/10.1016/j.molcel.2023.02.004